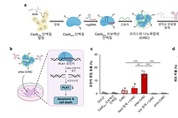
[더테크=조재호 기자] 카이스트가 유전자 가위 기술 기반의 항암 신약 기술을 개발했다. 이번 연구를 기반으로 유전자 교정 치료 및 다양한 암종에 적용할 수 있는 플랫폼 기술로 기대된다. 카이스트는 8일 정현정 생명과학과 교수 연구팀이 항암 신약을 개발해 암세포 선택적 유전자 교정 및 항암 효능을 보였다고 밝혔다. 이번 신약은 크리스퍼(유전자 가위) 기반 표적 치료제로 항체를 이용한 크리스퍼 단백질을 생체 내 표적 조직에 특이적으로 전달하는 방법이다. 유전자 치료에 사용하는 바이러스 기반 전달 방법은 인체 내 면역 부작용이나 발암성 등 한계점을 지녔다. 이에 비 바이러스성 전달 방법으로 단백질 기반의 크리스퍼 기술이 전달은 높은 안정성을 지녀 치료제로서 개발이 적합한 방법으로 알려졌다. 하지만 크리스퍼 단백질은 분자량이 커 전달체의 탑재가 어렵고 전달체의 세포 독성 문제 및 낮은 표적 세포로의 전달에 있어 어려움이 있었다. 이러한 문제점을 극복하기 위해 연구팀은 크리스퍼 단백질에 특정 아미노산을 변경해 다양한 생체분자를 보다 많이 결합하고 생체 내 본질적인 생화학 과정을 방해하지 않는 단백질을 개발했다. 그 결과 기존 비 바이러스성 전달체의 문제 해결 및 표적

[더테크=조재호 기자] 카이스트가 유전자 치료제 개발에 핵심 기술 중 하나인 유전자가위를 정밀 제어할 수 있는 기술을 개발했다. 향후 돌연변이를 표적으로 하는 RNA 기반 치료법과 세포 내 RNA 연구에 적용이 기대된다. 카이스트는 7일 허원도 생명과학과 교수 연구팀이 세계 최초로 RNA 유전자가위(CRISPR/Cas13)의 정밀 제어 기술을 개발하고 동물 모델에 적용해 RNA 염기 편집 효과를 입증했다고 밝혔다. 허 교수팀은 구조가 알려지지 않은 단백질의 구조를 재구조화해 화학적 및 광유전학적으로 조절 가능한 Cas13 단백질 조각을 예측하고 개발하는데 성공했다. 이를 통해 RNA 분해 및 RNA 염기 편집을 실시간으로 유도하고 활성을 조절할 수 있음을 확인했다. 아울러 세계 최초로 실험 쥐 모델에 해당 시스템을 적용해 효과를 입증했다. 이번 연구는 유전자가위 시스템을 활용한 유도 가능한 RNA 조절 시스템 개발로 질병과 관련한 돌연변이를 표적으로 하는 RNA 기반 치료법의 발전 및 세포 내 RNA 기반 연구에 적용될 것으로 기대된다. 연구팀은 RNA 대상 편집 시스템에서 단백질의 상대적으로 큰 크기를 유전체 전달에 있어서 임상적 적용에 한계점을 가지고 있